-
+ 7 (700) 356-49-30
-
Адрес
-
Форма заявки
-
ЯзыкРусский язык







 Вернуться В Меню
Вернуться В Меню



Применимые ситуации
① Типичные сценарии, наиболее подходящие для TrueBeam
• Очаги со сложной формой или расположенные рядом с критически важными органами.
• Опухоли в грудной или брюшной полости, подверженные влиянию дыхательных движений.
• Несколько внутричерепных очагов, требующих одновременного лечения нескольких зон-мишеней.
② Часто встречающиеся нозологии
• Голова и шея: рак носоглотки, другие опухоли головы и шеи
• Грудная клетка: рак легких, рак молочной железы
• Пищеварительная система: рак пищевода, рак желудка, рак прямой кишки, первичный рак печени
• Гинекология: рак шейки матки, рак эндометрия
• Мочеполовая система: рак простаты
• Центральная нервная система: опухоли ЦНС
Ключевые преимущества
① Улучшенный контроль дыхательных движений для более точного облучения мишени
TrueBeam оснащён функциями управления движением, такими как дыхательная синхронизация, позволяющими отслеживать ритм дыхания. При лечении опухолей в грудной и брюшной полости, которые заметно смещаются с дыханием, система может проводить облучение в оптимальной фазе дыхательного цикла, обеспечивая более точное соответствие положению опухоли и минимизируя ненужное облучение окружающих здоровых тканей. В большинстве случаев продолжительное задерживание дыхания не требуется, что облегчает сотрудничество пациента и повышает комфорт.
② Более эффективное лечение, снижает дискомфорт от длительного удерживания позиции
TrueBeam использует высокоскоростное управление системой и стабильный поток луча, поддерживая эффективные методы доставки, такие как VMAT. Это сокращает продолжительность отдельных сеансов, снижая время и сложность удержания позиции. Такой подход повышает эффективность рабочего процесса и улучшает опыт пациента.
③ Концентрированное лечение множественных внутричерепных очагов, экономия времени и упрощение процесса
С технологией HyperArc TrueBeam достигает субмиллиметровой точности, что позволяет облучать несколько опухолей за один сеанс. Система автоматически выполняет каждый дуговой сегмент по плану без необходимости ручной коррекции кушетки во время лечения. Такой процесс эффективен и безопасен, значительно повышая эффективность лечения, особенно для сложных случаев, таких как множественные метастазы мозга, требующие высокоточной работы с несколькими мишенями.
④ Гибкий выбор технических подходов по локализации и цели, лучшее соответствие плана
Линейный ускоритель TrueBeam поддерживает различные методы радиотерапии, включая трёхмерную конформную радиотерапию (3D-CRT), лучевую терапию с модулированной интенсивностью (IMRT), вращающуюся модулированную лучевую терапию (VMAT), визуализированную радиотерапию (IGRT) и стереотаксическую радиотерапию (SBRT). Это позволяет врачам выбирать наиболее подходящий метод в зависимости от анатомического участка и особенностей мишени, обеспечивая пациенту более персонализированное и комфортное лечение.
Почему выбирают больницу Цзиньшачжоу?
Для иностранных пациентов самой большой проблемой часто является не наличие технологий, а возможность завершить лечение непрерывно в соответствии с планом в пределах ограниченного пребывания. В нашей больнице есть современная платформа для лучевой терапии, включающая три линейных ускорителя TrueBeam, а также разработан гибкий график и система распределения пациентов. Это минимизирует влияние обслуживания оборудования и других факторов на расписание лечения, сокращает неопределённое ожидание и повторные поездки, и помогает зарубежным пациентам гладко проходить ключевые обследования, планирование лучевой терапии и проведение фракционных процедур, делая временные затраты на лечение за границей более управляемыми.
С момента первого лечения HyperArc в октябре 2020 года наша больница постоянно развивает клиническую практику и накапливает опыт, постепенно формируя процедуру управления несколькими целевыми зонами, что обеспечивает зрелую поддержку для случаев с несколькими внутричерепными мишенями. Кроме того, наша больница интегрирует лучевую терапию, платформы визуализации и мультидисциплинарное сотрудничество MDT в единый путь, координируя принятие решений и выполнение лечения в рамках одной системы. Это улучшает трансграничную коммуникацию и непрерывность лечения, позволяя иностранным пациентам больше сосредоточиться на самом лечении и восстановлении.
Для обеспечения стандартизированного внедрения и непрерывного функционирования этого пути наша больница создала систему контроля качества всего процесса лучевой терапии. Контрольные точки установлены от проверки плана и верификации дозы до выполнения лечения, под надзором команды радиотерапевтов, физиков и техников, что гарантирует согласованность и прослеживаемость выполнения планов. Для иностранных пациентов это означает более контролируемый процесс лечения, более ясное общение и повышенное чувство уверенности.
Техническое определение
Система TrueBeam, внедрённая в нашей больнице, представляет собой новое поколение линейных ускорителей и является одной из самых передовых разработок в мире, объединяющей целый ряд новейших технологий. Она может применяться для различных задач, включая лучевую терапию и радиохирургию с визуальным контролем. Оснащённая технологией HyperArc нового поколения, система благодаря своей высокой точности и эффективности существенно повышает скорость и точность лечения опухолей, что позволяет использовать её для различных методов лучевой терапии и при лечении разных заболеваний.
HyperArc — это некомпланарная стереотаксическая радиохирургическая технология с одним изоцентром и несколькими мишенями, специально разработанная для лечения внутричерепных опухолей. Она отличается высокой точностью, высокой эффективностью и высокой степенью автоматизации. Обладая субмиллиметровой точностью, технология позволяет в течение примерно 10 минут выполнить стереотаксическое радиохирургическое облучение от нескольких до десятков метастатических очагов в головном мозге, предоставляя пациентам с множественными метастазами мозга больше возможностей для лечения.
Механизм действия
① Биологическое действие излучения
Высокоэнергетические рентгеновские лучи, генерируемые системой TrueBeam, проникают в ткани организма и повреждают генетический материал опухолевых клеток, что нарушает их способность к росту и делению. Лечение, как правило, проводится фракционно, что позволяет контролировать опухоль за счёт накопленной дозы и одновременно даёт нормальным тканям время на восстановление.
② Формирование дозы и визуализационная навигация
Система формирует и подаёт излучение в соответствии с утверждённым планом лечения. Технологии IMRT и VMAT обеспечивают пространственное формирование дозы за счёт работы многолепесткового коллиматора (MLC) в сочетании с вращением гентри и управлением мощностью дозы, что позволяет максимально точно охватывать мишень и соблюдать ограничения по органам риска. Перед каждым сеансом выполняется двумерная и/или трёхмерная визуализация с последующей проверкой и, при необходимости, коррекцией положения (IGRT), что повышает воспроизводимость лечения.
③ Респираторный гейтинг (управление дыхательными движениями)
Система с помощью дыхательных датчиков или инфракрасных камер отслеживает маркеры на поверхности тела пациента и в реальном времени регистрирует дыхательный сигнал. На основе соответствия дыхательных фаз и движения опухоли задаётся «дыхательное окно». Облучение автоматически включается, когда дыхание входит в это окно и положение опухоли максимально близко к запланированному, и приостанавливается при выходе из него, что снижает неопределённость позиционирования, связанную с дыхательными движениями.
④ HyperArc и лечение множественных внутричерепных очагов
HyperArc основана на некомпланарной стереотаксической радиохирургии VMAT с одним изоцентром, реализуемой на линейном ускорителе. Процесс планирования отличается высокой степенью автоматизации и включает автоматическую генерацию дуг, оптимизацию углов коллиматора и гентри, а также применение инструментов SRS NTO (Normal Tissue Objective, цель защиты нормальных тканей при стереотаксической радиохирургии) и ALDO (Automatic Lower Dose Objective, автоматическая цель снижения дозы). Это обеспечивает более высокую дозу внутри мишеней и быстрое падение дозы за их пределами, повышая воспроизводимость планов и согласованность выполнения при лечении множественных внутричерепных очагов и делая процесс более управляемым.
Процесс лечения
① Оценка и планирование лечения
На основании стадии заболевания, данных визуализации и общего состояния пациента оценивается целесообразность лучевой терапии, определяются цели и оптимальные сроки лечения. При необходимости случай рассматривается на MDT и согласуется с другими методами терапии.
② Фиксация положения и КТ-симуляция
Проводится фиксация положения пациента и КТ-симуляция в лечебной позиции (при показаниях с учётом дыхательных движений), что служит основой для планирования.
③ Контурирование мишени и назначение дозы
Выполняется контурирование мишени и органов риска, определяется предписанная доза и схема фракционирования.
④ Разработка, проверка и верификация плана
Создаются планы IMRT, VMAT или другие соответствующие варианты, которые проходят клиническую проверку и необходимую верификацию для обеспечения безопасности и выполнимости.
⑤ Проведение лечения
Один сеанс лечения обычно включает следующие четыре этапа (указанное время ориентировочное и может варьироваться в зависимости от области облучения и рабочего процесса):
• Точная укладка (примерно 5–8 минут): В фиксированном положении выполняется трёхмерная визуализация для проверки позиции перед облучением.
• Интеллектуальная коррекция (примерно 1–2 минуты): Текущие изображения сопоставляются с плановыми, при необходимости выполняется коррекция положения с использованием шестистепенной лечебной платформы для повышения точности.
• Прецизионное облучение (примерно 2–5 минут): Доза подаётся в соответствии с планом. При использовании VMAT лечебная система непрерывно вращается, обеспечивая модулированное облучение с разных углов при сохранении эффективности и конформности дозы.
• Быстрый выход (примерно 1 минута): После завершения облучения пациент может сразу покинуть лечебный стол и зал, как правило без дополнительного восстановительного этапа.
⑥ Реабилитация и наблюдение
После окончания лучевой терапии врач даёт рекомендации, назначаются регулярные контрольные осмотры для оценки эффективности лечения и побочных эффектов, при необходимости проводится коррекция тактики или симптоматическая терапия.
Часто задаваемые вопросы
① Требуется ли специальная подготовка к лучевой терапии TrueBeam?
Ответ: Перед началом лечения проводится клиническая оценка, симуляция и изготовление средств иммобилизации (например, термопластической маски). Пациенту необходимо пройти обследования, такие как КТ и МРТ, для уточнения локализации и объема опухоли. Во время лечения требуется сохранять стабильное положение тела. В ряде случаев применяется респираторный гейтинг, для чего пациенту может потребоваться предварительная тренировка дыхательного контроля.
② Сколько длится один сеанс, сколько сеансов требуется и нужно ли ложиться в стационар?
Ответ: Продолжительность одного сеанса обычно составляет около 7–8 минут. При использовании специальных технологий, таких как респираторный гейтинг, время может увеличиваться до 15–20 минут. Общее число сеансов и длительность курса зависят от типа опухоли, стадии заболевания и выбранного плана лечения. В большинстве случаев лечение проводится амбулаторно. Необходимость госпитализации определяется состоянием пациента и планом терапии. Медицинская команда даст соответствующие рекомендации.
③ Что делать при появлении дискомфорта или изменении графика лечения?
Ответ: При возникновении дискомфорта или необходимости изменения расписания следует как можно раньше сообщить об этом лечащей команде. Обычно путем повторной оценки и корректировки графика удается сохранить непрерывность и безопасность курса лечения.
④ На что следует обратить внимание во время лечения?
Ответ: Необходимо соблюдать рекомендации врача по уходу за кожей в зоне облучения. Кожу следует содержать в чистоте и сухости. Следует избегать трения, горячих или холодных компрессов, расчесывания и применения раздражающих средств. Рекомендуется легкая, легко усваиваемая пища, достаточное потребление жидкости, а также корректировка режима дня и физической активности в зависимости от самочувствия.
⑤ Можно ли вести обычный образ жизни во время лучевой терапии?
Ответ: Как правило, пациенты могут сохранять определенный уровень привычной активности. Рекомендуется поддерживать тесный контакт с лечащим врачом и корректировать ритм жизни в соответствии с физическим состоянием. При появлении выраженных побочных эффектов, таких как стойкая слабость, повреждение кожи или повышение температуры, необходимо немедленно связаться с медицинским персоналом и временно ограничить обычную активность, отдавая приоритет здоровью.
Типичный случай
① Случай 1:
Пациентка, 38 лет
Комплексное лечение рака прямой кишки на протяжении почти 3 лет, головные боли в течение более 1 месяца.
Диагноз: Множественные метастазы в головной мозг при раке прямой кишки (стадия IVB, HER-2-положительный). Ранее проведённая химиотерапия и таргетная терапия оказались неэффективными, выявлены множественные внутримозговые метастатические очаги.
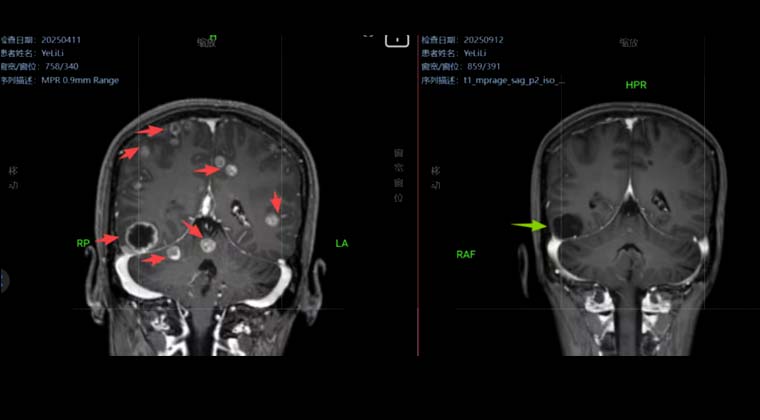
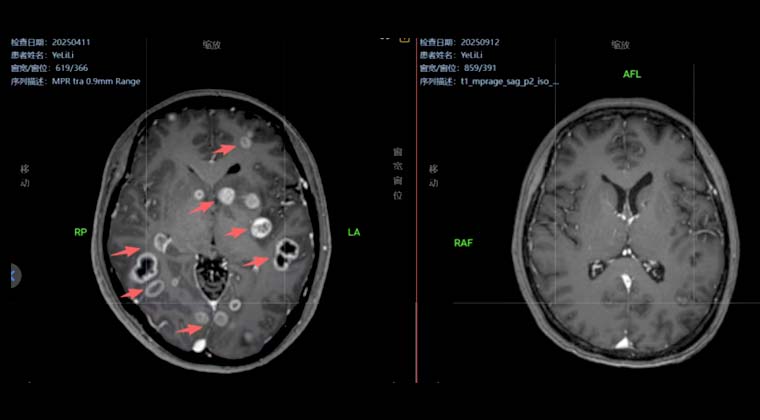
В апреле 2025 года в нашей клинике выполнена SBRT (стереотаксическая радиохирургия HyperArc) по поводу очагов в головном мозге, 40 Гр / 10 фракций.
Через 5 месяцев после лечения контрольное МРТ головного мозга показало практически полное исчезновение опухолевых очагов (G-PR). Качество жизни пациентки хорошее.
Изображение слева: до лечения
Изображение справа: после лечения
② Случай 2:
Пациентка, 76 лет
Диагноз «рак носоглотки» был поставлен 5 лет назад; стандартная химиолучевая терапия не проводилась, лечение осуществлялось самостоятельно. Месяц назад головные боли стали прогрессирующими и невыносимыми, сопровождались опущением левого века и снижением слуха.
Пациентка и семья попросили облегчить симптомы и уменьшить боль, отказавшись от химиотерапии. Была проведена паллиативная лучевая терапия локального очага опухоли. Опухоль оказывала давление на продолговатый мозг, поэтому была назначена доза 50 Гр / 25 фракций.
После 7 сеансов лучевой терапии опухоль значительно уменьшилась (на изображении область опухоли обозначена красной сплошной линией), головная боль облегчилась. У пациентки повысилась уверенность в лечении. План лучевой терапии был скорректирован для облучения шейной зоны лимфатического дренажа, и в итоге локальная опухоль получила суммарную радикальную дозу 70 Гр.
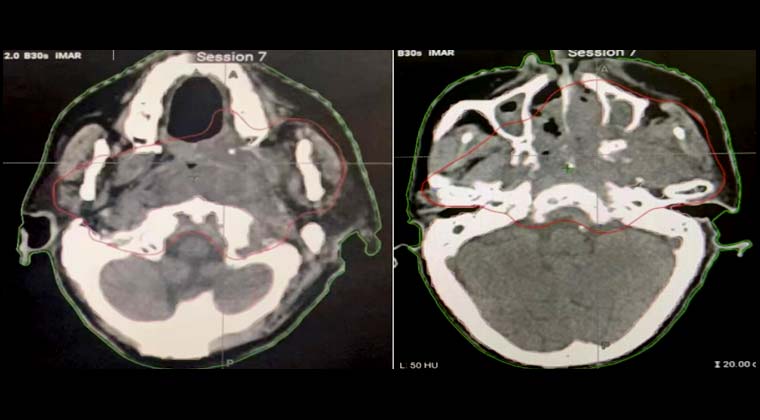
До лечения
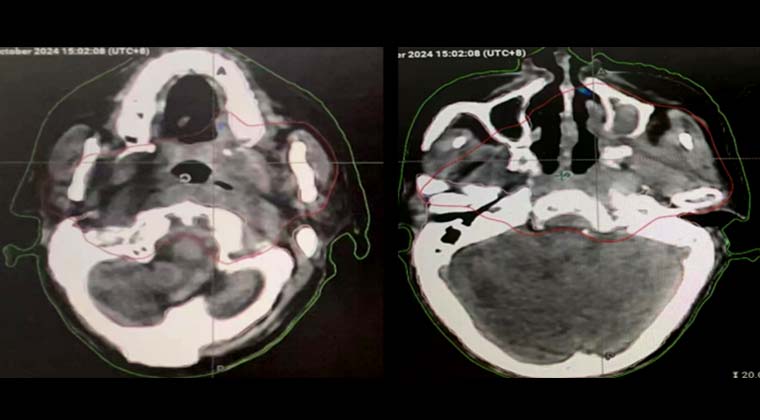
После 7 сеансов лучевой терапии
③ Случай 3:
Пациент: мужчина, 66 лет
Злокачественная опухоль носоглотки (недифференцированная некератинизирующая карцинома носоглотки)
С 102021 по 202021 проведена лучевая терапия методом VMAT (PGTV 69,96 Гр / 2,12 Гр / 33 сеанса)
После лечения проводилось непрерывное наблюдение, выявившее постепенное уменьшение опухоли в носоглотке.
При повторном МРТ 002023 отмечено исчезновение опухоли носоглотки и значительное уменьшение лимфатических узлов с ранее положительным диагнозом.
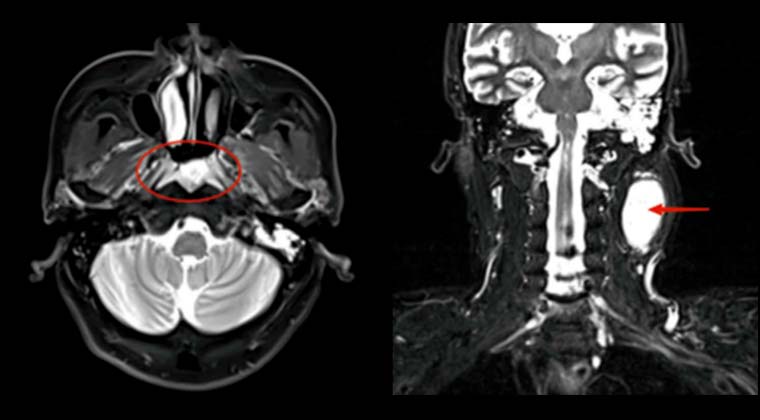
До лечения:
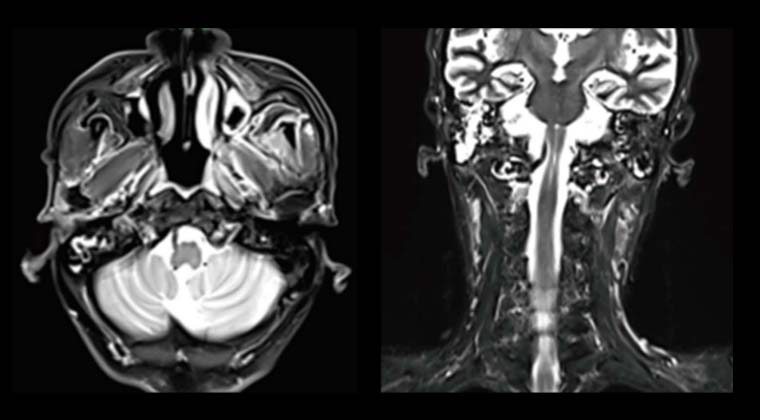
После лечения:
④ Случай 4:
Пациент: мужчина, пожилого возраста
Рак легкого с метастазами в мозг, нарушение функции мозга, использует инвалидное кресло
До лечения: выраженный отёк вокруг опухоли и повышенное внутричерепное давление
После лечения: опухоль уменьшилась после 5 сеансов лучевой терапии
После лечения функция мозга восстановилась; пациент смог самостоятельно ходить
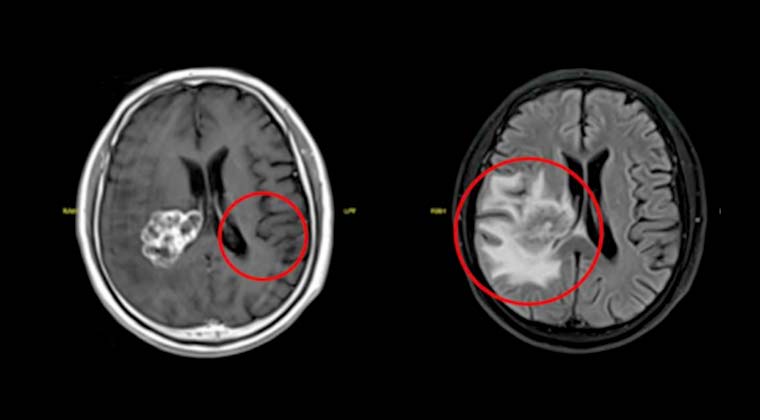
До лечения:
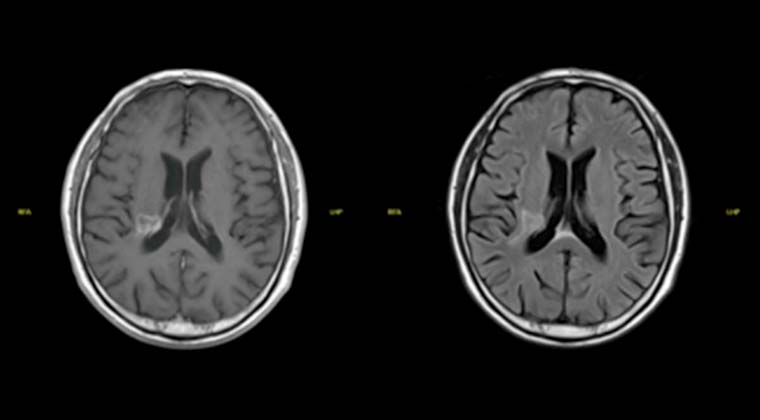
После лечения:
